-
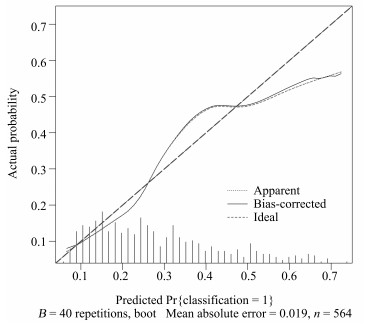
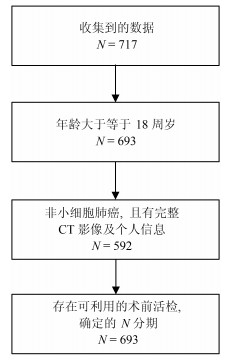
摘要: 在非小细胞肺癌的临床诊疗中,淋巴结是否转移对于医生制定手术方案有重要指导意义.但是目前临床上缺乏能够安全准确地预测非小细胞肺癌淋巴结转移的方法.本文应用影像组学方法对肺部CT影像进行定量分析来实现对非小细胞肺癌淋巴结是否转移的预测.从广东省人民医院收集了564例满足分析要求的非小细胞肺癌病例数据,并从每例CT影像中提取了386个定量影像特征,包括肿瘤的三维形状特征,表面纹理特征,Gabor特征以及小波特征:然后利用Lasso logistic regression(LLR)来构造非小细胞肺癌淋巴结转移的影像组学标签(Rad-score),并结合临床信息进行多元分析,构造了诺模图个性化预测模型.其中,LLR淋巴结转移预测模型性能在训练集上AUC为0.710,测试集AUC为0.712:在个性化诺模图上,用所有数据进行预测,得到C-index为0.724(95% CI:0.678~0.770),在一致性曲线上表现较佳,可为临床决策提供有价值的信息.Abstract: In the clinical diagnosis and treatment of non-small cell lung cancer, it makes great sense for guiding doctors to make operation plans according to lymph node metastasis status. However, a current weak point in clinical is the lack of a method that can be used to predict lymph node metastasis for non-small cell lung cancer safely and accurately. In this article, radiomic method was applied to the lung CT images to achieve quantitative analysis for the prediction of lymph node metastasis for non-small cell lung cancer. We collected 564 non-small cell lung cancer cases that could satisfy the data recruitment from Guangdong General Hospital, from which 386 quantitative radiomic features were extracted each, including the tumor's three-dimensional shape features, texture features, Gabor features and wavelet features. Then, Lasso logistic regression (LLR) was used to construct the radiomic signature (Rad-score) for the lymph node metastasis of NSCLC. With multivariate analysis of clinical information, the customized prediction nomogram model was built. The performance of the LLR model was shown to have an AUC of 0.710 in the training set and 0.712 in the validation set. Our nomogram model had a C-index of 0.724 (95% CI:0.678~0.770) and performed well on the consistency, providing valuable information for clinical decision-making.
-
Key words:
- Radiomics /
- lymph node metastasis /
- Lasso logistic regression /
- nomogram /
- calibration curve
1) 本文责任编委 朱朝 -
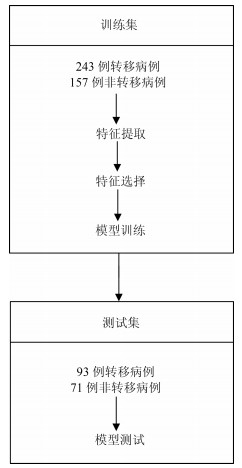
表 1 训练集和测试集病人的基本情况
Table 1 Basic information of patients in the training set and test set
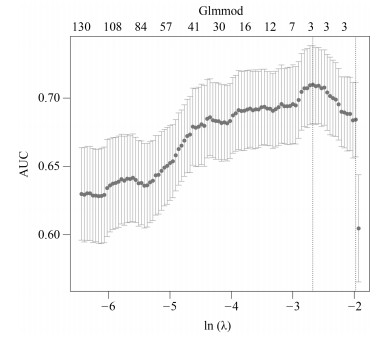
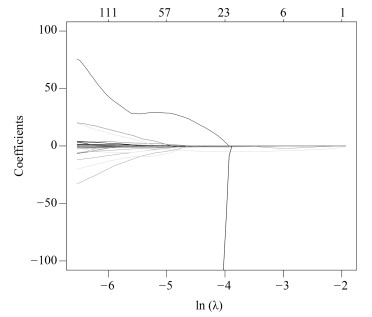
基本项 训练集($N=400$) $P$值 测试集($N=164$) $P$值 性别 男 144 (36 %) 0.896 78 (47.6 %) 0.585 女 256 (64 %) 86 (52.4 %) 吸烟 是 126 (31.5 %) 0.030* 45 (27.4 %) 0.081 否 274 (68.5 %) 119 (72.6 %) EGFR 缺失 36 (9 %) 4 (2.4 %) 突变 138 (34.5 %) $ < $0.001* 67 (40.9 %) 0.112 正常 226 (56.5 %) 93 (56.7 %) 表 2 Lasso选择得到的参数
Table 2 Parameters selected by Lasso
Lasso选择的参数 含义 数值 $P$值 $V0$ 截距项 2.079115 $V179$ 横向小波分解90度共生矩阵Contrast特征(Contrast_2_90) 0.0000087 < 0.001*** $V230$ 横向小波分解90度共生矩阵Entropy特征(Entropy_3_180) $-$3.573315 < 0.001*** $V591$ 表面积与体积的比例(Surface to volume ratio) $-$1.411426 < 0.001*** 表 3 不同方法对比结果
Table 3 Comparison results of different methods
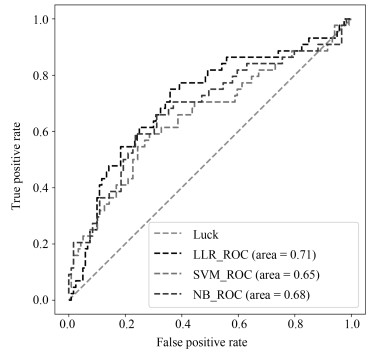
方法 训练集(AUC) 测试集(AUC) 召回率 LLR 0.710 0.712 0.75 SVM 0.698 0.654 0.75 NB 0.718 0.681 0.74 -
[1] Jemal A, Bray F, Center M M, Ferlay J, Ward E, Forman D. Global cancer statistics. CA Cancer Journal for Clinicians, 2011, 61(2):69-90 doi: 10.3322/caac.v61:2 [2] Howlader N, Noone A M, Krapcho M, Neyman N, Aminou R, Waldron W, et al. SEER cancer statistics review, 1975-2008. Bethesda, MD:National Cancer Institute[Online], available:http://seer.cancer.gov/csr/1975_2008/, August 1, 2015 [3] Glasgow S C, Bleier J I S, Burgart L J, Finne C O, Lowry A C. Meta-analysis of histopathological features of primary colorectal cancers that predict lymph node metastases. Journal of Gastrointestinal Surgery, 2012, 16(5):1019-1028 doi: 10.1007/s11605-012-1827-4 [4] Smith A J, Driman D K, Spithoff K, Hunter A, McLeod R S, Simunovic M, et al. Guideline for optimization of colorectal cancer surgery and pathology. Journal of Surgical Oncology, 2010, 101(1):5-12 doi: 10.1002/(ISSN)1096-9098 [5] Toiyama Y, Inoue Y, Shimura T, Fujikawa H, Saigusa S, Hiro J, et al. Serum angiopoietin-like protein 2 improves preoperative detection of lymph node metastasis in colorectal cancer. Anticancer Research, 2015, 35(5):2849-2856 http://www.wanfangdata.com.cn/details/detail.do?_type=perio&id=257db21275433b4ca2fe9da0f66d802c [6] Song J, Liu Z, Zhong W, Ma Z, Dong D, Liang C, et al. Nonsmall cell lung cancer:quantitative phenotypic analysis of CT images as a potential marker of prognosis. Scientific Reports, 2016, 6(1):Article No. 38282 doi: 10.1038/srep38282 [7] Gillies R J, Kinahan P E, Hricak H. Radiomics:images are more than pictures, they are data. Radiology, 2016, 278(2):563-577 doi: 10.1148/radiol.2015151169 [8] Kuo M D, Gollub J, Sirlin C B, Ooi C, Chen X. Radiogenomic analysis to identify imaging phenotypes associated with drug response gene expression programs in hepatocellular carcinoma. Journal of Vascular and Interventional Radiology, 2007, 18(7):821-830 doi: 10.1016/j.jvir.2007.04.031 [9] Lambin P, Rios-Velazquez E, Leijenaar R, Carvalho S, van Stiphout R G, Granton P, et al. Radiomics:extracting more information from medical images using advanced feature analysis. European Journal of Cancer, 2012, 48(4):441-446 doi: 10.1016/j.ejca.2011.11.036 [10] Sauerbrei W, Royston P, Binder H. Selection of important variables and determination of functional form for continuous predictors in multivariable model building. Statistics in Medicine, 2007, 26(30):5512-5528 doi: 10.1002/(ISSN)1097-0258 [11] Song J D, Yang C Y, Fan L, Wang K, Yang F, Liu S Y, et al. Lung lesion extraction using a toboggan based growing automatic segmentation approach. IEEE Transactions on Medical Imaging, 2015, 35(1):337-353 http://www.wanfangdata.com.cn/details/detail.do?_type=perio&id=25538c05c98e59d5f264491e0cd769c9 [12] Aerts H J W L, Velazquez E R, Leijenaar R T H, Parmar C, Grossmann P, Carvalho S, et al. Decoding tumour phenotype by noninvasive imaging using a quantitative radiomics approach. Nature Communications, 2014, 5:Article No. 4006 doi: 10.1038/ncomms5006 [13] Vickers A J, Cronin A M, Elkin E B, Gonen M. Extensions to decision curve analysis, a novel method for evaluating diagnostic tests, prediction models and molecular markers. BMC Medical Informatics and Decision Making, 2008, 8:Article No. 53 doi: 10.1186/1472-6947-8-53 [14] Zhang L J, Yang T B, Jin R, Zhou Z H. Stochastic proximal gradient descent for nuclear norm regularization. arXiv:1511.01664v2, January 1, 2015 [15] Huang Y Q, Liang C H, He L, Tian J, Liang C S, Chen X, et al. Development and validation of a radiomics nomogram for preoperative prediction of lymph node metastasis in colorectal cancer. Journal of Clinical Oncology, 2016, 34(18):2157-2164 doi: 10.1200/JCO.2015.65.9128 [16] Liang W H, Zhang L, Jiang G N, Wang Q, Liu L X, Liu D R, et al. Development and validation of a nomogram for predicting survival in patients with resected non-small-cell lung cancer. Journal of Clinical Oncology, 2015, 33(8):861-869 doi: 10.1200/JCO.2014.56.6661 -




 下载:
下载: